第4章
化学变化 在电池
在解释中的一个存储单元会发生什么,让我们看看到蓄电池的早期历史,看看什么是谦虚开始了现代重型电池了。 与1850年和1860年一个名为普兰特的人开始了他对蓄电池的工作。 他的原始细胞包括金属铅两板浸泡在稀硫酸。 酸形成的薄层硫酸铅在其即将停止在引线进一步行动各板。 如果一个电流通过电解池,对“ 阳极 ”或在其中电流进入电池的引线板的硫酸铅被改变成过氧化铅,而在另一引线板或“ 阴极 ”硫酸盐变更为纯引领海绵状的形式。 此细胞静置数天,然后“排出”,硫酸铅被再次对每块板形成。 每次该电池充电,更多的“海绵”铅与过氧化铅形成。 这些被称为“活性”材料,因为它是通过它们与该电力生产的硫酸之间的化学作用。 显然,板所含的多种活性物质,更长的酸和活性物质之间的化学作用可能发生,并因此更大的“容量”,电力公司提供的细胞或量。 的充电和放电的电池,以增加活性材料的量,该过程被称为“ 形成 ”的板中。成形板普兰特的方法是很慢的,乏味的,且价格昂贵。 如果海绵状铅和氧化铅的可能迅速地从材料可能被散布在板,大量的时间和费用可以节省下来进行。 这是福雷谁第一个提出这样的计划,并给我们的“ 粘贴 ”板块今天,它由一个骨架框架的铅,用海绵铅的铅与过氧化填充框架的“肋骨”之间的空间。 这种板被称为“粘贴”板,和轻得多和更令人满意的,对于汽车的工作比普兰特的沉重的固体导线板。 第3章说明更加充分地制造和粘贴板的工艺。
|
|
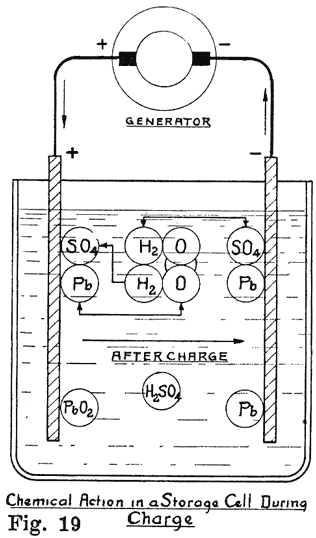
上面的描述给出了所发生的二次电池的化学变化的最终产品。 了解自己的变化,需要更详细的调查。 在化学作用被认为是物质是硫酸,水,纯铅,硫酸铅,铅过氧化物。 除了纯铅,每一种物质,是一种化学化合物,或几种元素所组成。 因而硫酸是由氢,这是一个气体两部分组成; 一个部分的硫,固体,和4份氧,这也是一个气体; 这些结合形成的酸,这是液体,并且其是为了方便起见表示为H 2 SO 4,H 2代表氢两部分组成,S 1部分的硫,和0 4,4份氧。 类似地,水是液体,是由氢气的两部分和一个氧部分,用符号H 2 O表示的 铅是不是一种化合物,而是一个元素,它的化学符号是Pb计,从铅的拉丁名服用。 硫酸铅是一种固体,它由一个零件中的铅,一种固体物质,硫的一部分,另一种固体物质,和4份氧的气体的。 它是由铅SO 4化学上表示。 过氧化铅也是一个固体,而且是由一个零件中的铅,和氧的两部分。 中所发生的化学变化,刚才所描述的化合物可在一定程度上分裂成其中它们构成的物质。 因此,我们有铅(Pb),氢(H),氧(O),硫(S),4基本物质,其中两个是固体,并且两种气体。 硫不完全从与它构成了化合物的H 2 SO 4和Pb SO 4的物质的分离本身。 这些化合物被分裂成H 2和SO 4和Pb分别SO 4。 即,硫始终保持组合与4份氧。现在让我们考虑由电解质的单个存储单元,一个正极板和一个负极板。 当此电池完全充电,或在条件以产生电力的电流,正极板由过氧化铅(PbO的2),纯铅(Pb),负极板组成的,并且稀硫酸的电解液(H 2 SO 4)。 这示意在图 19。 这发生时,电池放电和变化的最终结果是如下的化学变化:
(一)。 在正极板:过氧化铅和硫酸产生的硫酸铅,水和氧气,或:
![]()
(b)所示。 在负极板:铅和硫酸产生的硫酸铅和氢气,或:
![]()
方程(a)和方程的氢的氧(B)相结合,形成水,因为可通过添加这两个方程,得到方程1为整个放电动作显示:
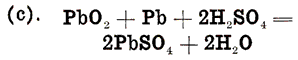
在此公式中,我们开始与活性材料和电解质在其原始状态,并完成与硫酸铅和水, - 这是一个放电的最终产品。 研究这个方程,我们可以看到,电解液的硫酸用于在两个正极和负极板形成硫酸铅,因此被从电解液中移除。 这给我们的回忆放电动作,这虽然开放,从严格的科学观点提出质疑,仍然是方便易记的规则: | |
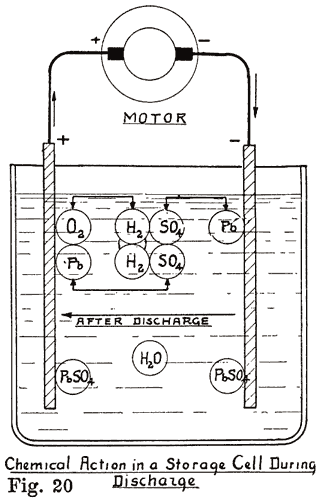
采取在其放电状态的电池,现在让我们小区连接到一台发电机和发送电流通过该槽从正极到负极板,这被称为“充电”的单元格。 硫酸铅和水现在将逐渐变回成铅,过氧化铅和硫酸。 硫酸铅是在负极板上被改变为纯铅; 在正极板中的硫酸铅被改变到导致过氧化物和硫酸将被加入到水中时 , 在正极板的变化可如下表示:硫酸铅和水产生。 硫酸,氢和过氧化铅,或:
![]()
在负极板上的变化可以表示为如下:硫酸铅和水生产硫酸,氧和铅,或:
![]()
在负极板上产生的氢气(H 2)在正极板产生的,和氧(0)结合形成水,如可以由下式所示:
![]()
式(F)开始,硫酸铅和水,其中,如式(c)所示,是当电池被放电产生的。 将观察到,我们先从硫酸铅和水。 排出板因此可带电水。 事实上,很糟糕排出底片可充电更好在水中比在电解质。 电解液倒出电池和蒸馏水倒入英寸残留在分离器和板的酸足以使水进行的充电电流。在等式(f)中 ,在平板上的硫酸盐与水结合形成硫酸。 这给我们的规则:
在充电过程中,酸是。 赶出板。这个规则是一个方便的一个,但,当然,不是严格正确的说法。
通过发送一个电流通过电池产生的变化也逐渐的,并且将发生更快的电流变得更大。 当所有的硫酸铅已被“用完引起的电流的化学变化,没有进一步的充电才能进行。 如果我们继续发送电流通过该单元之后,它被完全充电时,水将继续被分解成氢气和氧气。 然而,因为没有更多的硫酸铅左与该氢气和氧气可结合形成铅,过氧化铅和硫酸,氢,氧引起的电解质的表面并从细胞逃脱。 这就是所谓的“ 毒气 ”,并且是一个迹象表明,电池完全充电。
现在我们知道,在电池产生电力,并且化学作用,另一方面,电流,通过从外部源,例如发电机,电池送出,产生在电池的化学变化。 怎样的化学变化和电有关系吗? 我们有在电池的各种化学元素都应该携带小电荷的电力,其中,但是,通常中和彼此。 当一个单元被放电,但是,电解质,水和活性物质被分离成多个部分进行负电荷和正电荷,而这些“费用”的原因就是我们所说的电流流入连接至电池装置。类似地,当。 电池充电时,充电电流产生的电“罪名”,这引起电池的物质团结起来,由于位置和负电荷彼此的吸引力。 这是化学反应和电的电池之间的关系进行了简要,粗略的说法。 这个问题的更深入的研究将是不合时宜的,在这本书。 它是足够的修理工要记住,在电的电池进荷,成为可作为电流时的电池放电,而充电电流引起的电荷形成,从而“充电”电池中的物质。